北京时间10月6日起,2025年诺贝尔奖将陆续揭晓,生理学或医学奖一如既往牵动医疗圈与患者家庭的心。官方日程已确认,但诺奖提名严格保密,外界所有“名单”都只是合理推测。

(来源:摄图网)
本文站在“向愈集”读者(肿瘤患者与家属)的视角,梳理有希望获得2025年诺贝尔医学奖的、与肿瘤直接相关的几个方向,并解释:这些成果改变了什么?为什么“值得被诺奖看见?”
最强热门:CAR-T细胞疗法的奠基者们
你可以把CAR-T理解为“给患者自家T细胞装上GPS与导弹”。医生先把你的T细胞取出来,在实验室里装上一段能精准识别癌细胞的“嵌合抗原受体”(CAR),再把武装后的T细胞回输体内去追杀肿瘤。
CAR-T的诞生,已经把多种血液肿瘤的治疗天花板,一次次撞开了。
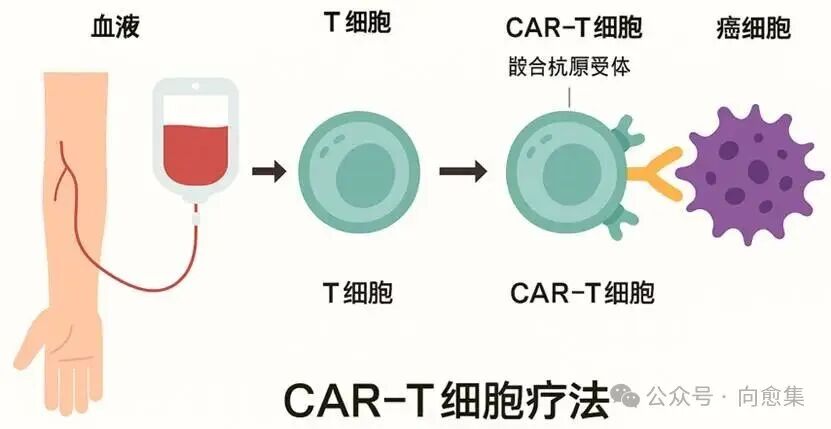
CAR-T细胞疗法(来源:AI生成)
为什么今年“很有机会”?
跨大奖的充分预热:近年CAR-T先驱Carl June与Michel Sadelain已拿下“科学界奥斯卡”突破奖等顶级荣誉,通常被视作诺奖的强烈风向信号。
临床影响力坐实:欧洲与美国已批准6款CAR-T用于白血病、淋巴瘤、多发性骨髓瘤等(疗效好但也昂贵、并发症需严密管理)。
从“血液肿瘤”向“实体瘤”突围的里程碑:2025年ASCO期间公布的全球首个实体瘤CAR-T随机对照试验(胃癌/胃食管交界癌)显示,总生存期较标准治疗延长约40%,意义重大。
一句话说:CAR-T让部分“药石罔效”的血液瘤患者实现了长程无复发,未来实体瘤管线还正在加速;它不是“包治百病”的神药,但作为一种全新治疗范式,已经改写了无数家庭的剧本。

全球首个CAR-T治疗的白血病患儿Emily,已无癌生存13年
可能的诺奖“组合”:CAR-T的“发明-工程化-临床验证”链条很长,除Carl June与Michel Sadelain外,Zelig Eshhar(早期概念与原型)也常被提及。
无论获奖者是谁,CAR-T体系性贡献本身,已具备诺奖级别的“范式革命”特征。
直面“难打的癌基因”:KRAS抑制剂的开路者
在肿瘤学里,KRAS曾被称作“不可成药的铁王座”。
如今,“铁王座”被打破:Kevan Shokat团队用“化学机关”卡住了KRAS-G12C这处“活门”,首开直接抑制KRAS的先河,继而促成首批KRAS抑制剂问世(如Sotorasib在2021年获FDA加速批准,Adagrasib在2022年获批),让部分晚期肺癌等患者出现转机。
全球首个获批的KRAS靶向药Sotorasib(Lumakras)
你可以把它想象成:几十年打不开的锈死门锁,被精准打磨的一把钥匙成功开启。
为什么今年“也有机会”?
科学难度极高:近40年全球努力未果,直到“共价小分子”策略击中了G12C这个“阿喀琉斯之踵”。
临床已落地:KRAS抑制剂相继获批进入临床,打开了“从不可成药到可成药”的大门,间接激活了KRAS其他突变位点(G12D等)和联合方案的开发热潮。
KRAS突变常见于肺癌、结直肠癌、胰腺癌等“硬骨头”。
从“无药可用”到“有靶点药”,意味着多一条走下去的路。当然,耐药与人群获益的精细分层仍是下一阶段的攻坚。
以“合成致死”撬动精准治疗:PARP抑制剂与BRCA
把肿瘤比作一座有两套电路的工厂:BRCA通路坏了(DNA同源重组修复缺陷),工厂勉强靠PARP通路供电维持。科学家灵感一闪:把PARP再切掉,癌细胞就“全黑”——这就是“合成致死”。
2005年两篇里程碑论文(Bryant et al.;Farmer et al.)首次证实了这一策略,随后奥拉帕利(olaparib)于2014年成为全球首个获批的PARP抑制剂,此后扩展到乳腺、前列腺、胰腺等多癌种,真正把“分子脆弱性”转化成了患者获益。

全球首个获批的PARP抑制剂奥拉帕利(olaparib)
为什么说具备“诺奖相”?
把“基因修复缺陷→药物敏感”的因果链条打通,定义了一整类精准治疗范式;
持续的临床扩张与真实世界证据,证明这不是“学术一闪”,而是可复制的治疗策略。
当患者体内携带BRCA/HRD等特定改变,医生即可推荐使用PARP抑制剂(有时与免疫、抗血管药联用)。它并非人人适用,但对合适人群,疗效与生活质量兼顾的价值已被反复验证。
从影像到“定点清除”:PSMA放射配体治疗(RLT)
可以把它想象成“会找路的微型放射源”:PSMA-617这把“寻靶钥匙”与锥形弹头^177Lu结合,专找前列腺癌细胞“下手”。
关键III期VISION研究显示:在标准治疗基础上联合PSMA-617,患者总生存与影像学无进展生存显著改善;随后Pluvicto(^177Lu-PSMA-617)于2022年3月获FDA批准,成为首个获批的PSMA靶向放射配体疗法,加速了前列腺癌“诊疗一体化(theranostics)”路径的落地。
前列腺癌放射性配体疗法Pluvicto
在2024美国泌尿外科协会年会上,研究人员又公布了Pluvicto(^177Lu-PSMA-617)的3期临床试验结果:患者的放射学无进展生存期提高了1倍多,获得完全缓解的比例是活性对照组的接近8倍。
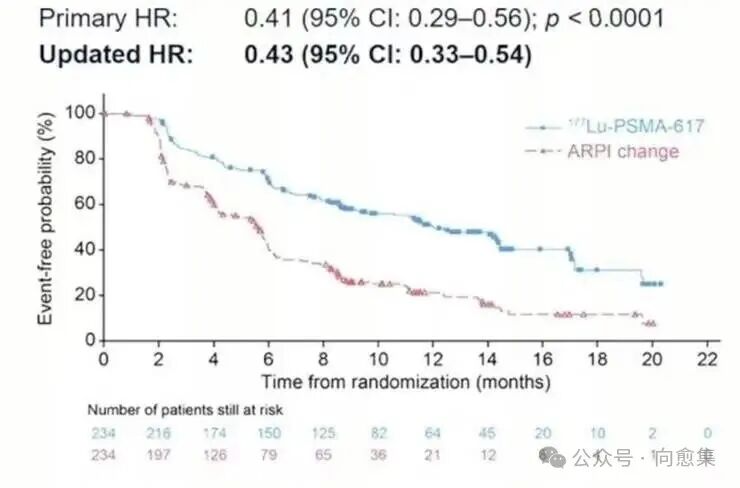
Pluvicto显著改善患者无进展生存期
为什么也值得被关注为“黑马”?
从德国学术源头到全球标准,完整走通“影像探针→治疗配体→生存获益”的转化链路;
技术平台外溢性强,RLT已在探索更多靶点,给实体瘤提供了与手术、药物并列的第三种系统性打击方式。
其他若干“潜在话题奖”与合议
除了上面四大“硬核方向”,还存在一些可能以“话题串奖”或“长期贡献”方式被关注的肿瘤相关领域。
诸如:
ctDNA/液体活检与MRD:把“复发的影子”在血液里提前揪出来,指导辅助治疗“加或减”。II期结肠癌的DYNAMIC随机研究已证明:用ctDNA指导,可减少一半化疗而不损害无复发生存,真正把“少治与好治”兼得的图景落到实处。(MRD指“没清干净但肉眼检测不到”的癌细胞痕迹)
免疫治疗的广谱优化:2018年诺奖已表彰PD-1/CTLA-4,但如何让更多冷肿瘤“热起来”、如何预测与管理毒性,仍是未来可被“体系性贡献”认可的方向。相关综述指出,免疫治疗仍将是未来肿瘤治疗的“主旋律”。
结语:诺奖是里程碑,不是终点
诺奖强调“造福人类”,诺贝尔医学奖更是如此。

(来源:摄图网)
从这个角度看,上述四大方向都已满足“改变命运”的标准:
要么开创全新治疗范式(CAR-T、RLT)
要么攻克百年难题(KRAS)
要么把“精准医学”从纸面推到床边(PARP/BRCA、ctDNA-MRD)
今年的诺贝尔医学奖花落谁家,让我们静待10月6日揭晓。
但对患者与家属而言,更重要的是:及早完成分子分型、尽量进入规范路径、用上对的工具——这样,当科学抵达“诺奖时刻”,你已经在路上了。
说明:
诺奖不公开候选名单,本文仅基于公开可考的临床影响、跨大奖信号与学术共识做出面向患者的解读与预测,不构成投资建议与医疗处方;
具体治疗请遵医嘱与多学科会诊。
【盛诺一家】成立于2011年,是国内领先的海外医疗咨询服务机构,至今已为近10000个患者家庭提供出国就医服务,重点涵盖癌症、心脏病、罕见疾病等重疾领域。凭借专业、贴心、高效的服务,盛诺一家赢得了99%客户好评率!
📌为什么出国就医患者选择盛诺一家?
- 全球就医:覆盖中、美、英、日1000家医院网络,不局限于单一国家医疗资源、规划最优就医路径
- 专业可靠:咨询服务团队成员70%拥有医学背景,包括医学院博士、三甲医院医生、资深医学翻译
- 一站式服务:在全球设有15个客户服务中心,保障从国内到海外全流程、高品质的服务质量
- 客户至上:推出48小时冷静期、风险告知书、医疗费用“零加成”等措施,保障客户权益
- 专属折扣:通过本公司预约出国就医的患者,可额外申请5%–40%的医疗费用减免折扣
👉如果您或者家人需要出国看病,可拨打免费咨询热线 400-855-7089,或通过 盛诺一家官网 预约咨询!








