对于很多胃癌患者,尤其是晚期、HER2阴性的朋友来说,治疗选择一度非常有限。但这一状况正在不断改观。
据3月16日NovaBridge发布的官方新闻,美国食品药品监督管理局(FDA)正式确认,胃癌创新双抗药物Givastomig符合“加速审批”路径。
这意味着,这款新药有望缩短审批时间、更快来到患者身边。

(来源:NovaBridge)
什么是Givastomig?
它是胃癌战场的“特种兵”。
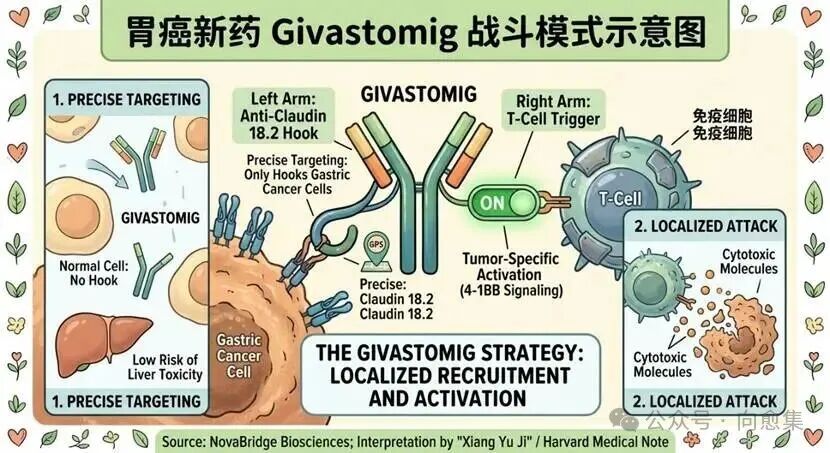
在医学界,Givastomig被称为Claudin 18.2 / 4-1BB双特异性抗体。听起来很复杂?其实它就像一个拥有“双重身份”的特种兵:
第一重身份:精准制导。它的一个“钩子”专门钩住胃癌细胞表面的Claudin 18.2(胃癌的一个重要靶点)。
第二重身份:就地扩招。它的另一个“钩子”抓住、激活人体自身的T细胞(免疫细胞)。
神奇的地方在于:以前类似的免疫增强药(4-1BB激动剂)因为副作用太大,会误伤肝脏。但Givastomig非常“聪明”,它只有在遇到胃癌细胞时才会激活。
它就像一个“只有在犯罪现场才会拉响的警报”,只在肿瘤局部动员免疫力量,有望大幅降低对全身的毒副作用。
(来源:Gemini)
75%的缓解率:这意味着什么?
在刚刚公布的临床数据中(Phase 1b研究),Givastomig联合化疗和免疫药物,在一线治疗中表现出色:
肿瘤显著缩小:客观缓解率(ORR)达到75%(其中8 mg/kg剂量组更是达到了77%)。也就是说,4个受试患者中,有3个肿瘤都明显缩小了。
不挑“体质”:以往的同类药物要求患者的靶点表达(Claudin 18.2)必须非常高。但数据显示,Givastomig在中低表达的患者中也观察到疗效信号。这意味着,更多原本“没药可用”的患者,可能拥有新机会。
生存期延长:中位无进展生存期(mPFS)达到了16.9个月,这一结果在当前研究中令人鼓舞。
FDA“加速审批”,希望近在咫尺
FDA确认其“加速审批”资格,是一个重大的监管信号。

通常,药物上市需要观察几年的“总生存期”数据。但因为Givastomig表现出色,FDA允许厂家使用“客观缓解率(肿瘤缩小的比例)”作为主要指标来申请上市,有望比常规路径提前获批。
但该有的动作不会停,全球多中心的大规模III期临床试验预计将在2026年第四季度正式启动。
结语:
胃癌曾被称为“穷人癌”,晚期治疗方案一度停滞不前。但从免疫治疗,到现在的“双抗”技术,医学正在一点点收复失地。
Givastomig的出现,给了我们一个清晰的信号:未来的胃癌治疗将更加精准、低毒且高效。
如果您或您的家人正在与胃癌战斗,请保持信心。科学发展的速度,往往比我们预想的还要快。
参考来源:
1.NovaBridge Biosciences. (2026, March 16). NovaBridge Announces Productive FDA Type B Meeting on Potential Accelerated Approval Pathway for Givastomig in Gastric Cancer.
2.ClinicalTrials.gov. Study of TJ033721 (Givastomig) in Subjects With Advanced or Metastatic Solid Tumors. Identifier: NCT04900818.
3.Targeted Oncology. (2026, March 16). FDA Confirms Potential Accelerated Path for Givastomig in GE Cancer.
【盛诺一家】成立于2011年,是国内领先的海外医疗咨询服务机构,至今已为近10000个患者家庭提供出国就医服务,重点涵盖癌症、心脏病、罕见疾病等重疾领域。凭借专业、贴心、高效的服务,盛诺一家赢得了99%客户好评率!
📌为什么出国就医患者选择盛诺一家?
- 全球就医:覆盖中、美、英、日1000家医院网络,不局限于单一国家医疗资源、规划最优就医路径
- 专业可靠:咨询服务团队成员70%拥有医学背景,包括医学院博士、三甲医院医生、资深医学翻译
- 一站式服务:在全球设有15个客户服务中心,保障从国内到海外全流程、高品质的服务质量
- 客户至上:推出48小时冷静期、风险告知书、医疗费用“零加成”等措施,保障客户权益
- 专属折扣:通过本公司预约出国就医的患者,可额外申请5%–40%的医疗费用减免折扣
👉如果您或者家人需要出国看病,可拨打免费咨询热线 400-855-7089,或通过 盛诺一家官网 预约咨询!








