在日本,药审机构PMDA每月都会发布“新医药品承认品目一览”。
在2025年9月的这份清单里,和肿瘤相关的条目格外亮眼:
既有小众但凶险的血液肿瘤新增免疫治疗适应症;
也有脑瘤、肺癌这样常见而棘手的实体瘤首个(或更新一代)靶向药;
更有放射性配体治疗与PSMA-PET成套“诊疗一体”的组合进入临床。
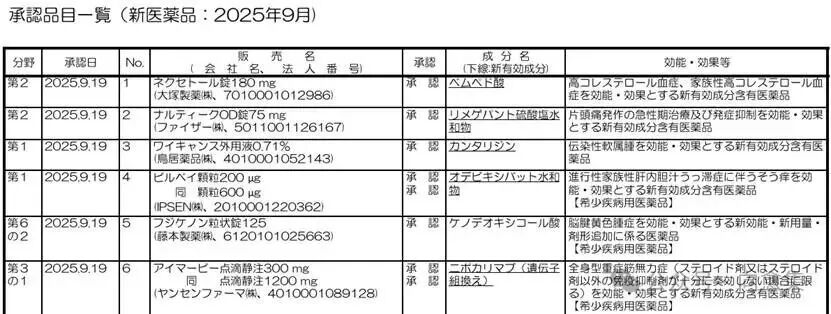
日本PMDA 2025年9月获批清单(部分)
对患者而言,这些变化不只是“药柜上多了几盒新药”,而是治疗路径真正被改写。
那么,日本9月具体批了啥?背后证据是否可靠?下面就为大家来捋一捋。
鼻型ENK/T细胞淋巴瘤:免疫治疗“补上短板”
日本把罗氏/中外(指日本中外製薬株式会社)的阿替利珠单抗(Atezolizumab,商品名Tecentriq)新增了一个适应症:复发/难治的节外性NK/T细胞淋巴瘤·鼻型(ENKTL)。
(AI生成,图片仅供参考)
这是一种罕见、进展快、复发后几乎无标准药物可选的血液肿瘤。过去,临床往往依赖含天冬酰胺酶方案或移植,选择有限、预后不佳;免疫检查点抑制剂虽有“零星”研究,但真正拿到适应症的并不多。
此次日本放行,核心依据是本土医师主导的ATTACKⅡ期研究:14例入组、13例可评,客观缓解率53.8%(独立评审),安全性与以往适应症相似。在日本,这有望成为首个获批用于ENKTL的免疫检查点药物。
对国内患者意味着什么?
国内临床上,ENKTL复发后常被迫在有限的化疗/放疗与移植之间“拼运气”。日本此次扩展说明:小样本但高质量的、本土主导证据也能撬动审评。而且,免疫治疗在这类EB病毒相关肿瘤上具备生物学合理性。后续若有更多真实世界数据,可能加速其他国家/地区的适应症推进。
低级别IDH突变胶质瘤:“首个专门药”从美国走到日本
沃拉西地尼(Vorasidenib;日本品牌名“ボラニゴ/ボラニゴ錠”,英文Voranigo)在日本获批用于IDH1或IDH2突变阳性的神经胶质瘤。
沃拉西地尼(Voranigo,来源:网络公开资料)
这类脑瘤以往主要靠手术+观察/放化疗,长期缺乏“专门靶向药”:
2024年8月,美国FDA率先批准Voranigo用于12岁及以上、术后随访期的2级星形细胞瘤或少突胶质细胞瘤患者,奠定“全球首个”地位;
决胜证据是随机Ⅲ期INDIGO研究:中位无进展生存期27.7个月,而安慰剂组只有11.1个月。
日本此次跟进,意味着东亚患者更早享有延缓复发的系统性药物。
对年轻、预后期望长的IDH突变低级别胶质瘤人群,延缓复发=延缓放化疗相关不良反应的到来,意味着工作、学习、生育计划都能多一份“时间红利”。
目前,Voranigo国内尚未上市,IDH小分子更多是围绕胆管癌/白血病等适应症的既有药;脑瘤专用的IDH双抑制剂在国内仍属空白。
非小细胞肺癌“两把快刀”:HER2突变与ROS1融合各就位
1.HER2突变非小细胞肺癌:Zongertinib“把副作用降低”
日本批准Zongertinib(BI-1810631;日本商品名“ヘルネクシオス/HERNEXEOS”),用于既往接受过化疗后进展的、HER2(ERBB2)基因变异阳性、不可切除进展/复发非小细胞肺癌患者。
(AI生成,图片仅供参考)
与既往“命中HER2但常误伤EGFR”的TKI(酪氨酸激酶抑制剂,肿瘤药物里常见的一大类“靶向药”)不同,Zongertinib是高选择性HER2抑制剂,旨在降低EGFR相关皮疹/腹泻与间质性肺疾病风险。
在2025年美国癌症研究协会(AACR)公布的研究中,其客观缓解率约71%,且耐受性优于早期同类。
HER2突变肺癌仅占所有肺癌的2%-4%,过去更多靠化疗或ADC药物(如T-DXd)“硬扛”,但ADC药物的间质性肺疾病等风险不容忽视。若能用口服、小分子、选择性强的方案解决一部分患者,疗效与安全性可能出现更好的平衡。
2.ROS1融合非小细胞肺癌:Taletrectinib“一线/耐药皆可打”的下一代
日本批准Taletrectinib(他雷替尼;日本商品名“イブトロジー/Ibtrozi”),用于ROS1融合阳性的不可切除进展/复发非小细胞肺癌。这是一代“更抗耐药、可过血脑屏障”的ROS1抑制剂。
(AI生成,图片仅供参考)
Taletrectinib的研发背景很独特,开始是由日本药企研发,2014年国内药企获得了该药的全球开发与商业化权利,随后主导了临床试验。由于国内患者基数大,率先在中国开展了关键注册临床试验。
2025年1月,国内率先批准Taletrectinib用于晚期ROS1阳性的成人非小细胞肺癌;6月,美国FDA也批准了相同的适应症。关键证据来自TRUST-I研究等:显示持久缓解与显著无进展生存期,且对脑转移有活性。
日本这次把Taletrectinib引进肺癌“武器库”,对既往克唑替尼后进展/脑转的难题,提供了新选择。
前列腺癌“诊疗一体化”落地:放射性配体治疗+PSMA-PET成套上新
这一块,日本9月一次性通过了三个关键件:
Pluvicto®(177Lu-vipivotide tetraxetan):针对PSMA阳性的去势抵抗性前列腺癌(mCRPC);
Locametz®(^68Ga-Gozetotide)试剂盒:用于PSMA靶向治疗的患者适应性判定(成像);
^68Ge/^68Ga发生器:保障医院端现场制备^68Ga示踪剂。
三者共同构成“诊断—治疗—再评估”的闭环。
今年3月,美国FDA已把Pluvicto的适应症前移到“化疗前”;日本此次批件,意味着更多晚期前列腺癌患者能用上全球证明有效的RLT(放射性配体治疗),与国际节奏同步。
Pluvicto(来源:网络公开资料)
这套“组合拳”到底有何价值呢?
更精准的筛选:先做PSMA-PET(如用Locametz),筛出真正表达PSMA的患者再给药,减少无效治疗;
系统性杀伤转移灶:Lu-177标记的配体全身“找灯”后,直接把β射线送达肿瘤位点,对骨转移尤其友好;
路径明确:发生器+试剂盒的引入,降低了医院配制门槛,使“诊疗一体化”能够真正落地。
给患者的“落地指南”:谁可能受益?
1.复发/难治性鼻型ENK/T细胞淋巴瘤:化疗/移植后乏力者,可咨询是否符合【阿替利珠单抗】用药条件。稀有病种,建议在有淋巴瘤专长中心评估。
2.IDH突变低级别胶质瘤(术后随访期):目标是延长无进展时间、推迟放化疗,可关注【沃拉西地尼】;尤其年轻患者,生活质量受益更突出。
3.HER2突变非小细胞肺癌:若曾用化疗或ADC药物且耐受欠佳,【Zongertinib】可提供口服、选择性强的替代路径。
4.ROS1融合阳性非小细胞肺癌:初治或耐药、以及脑转移风险高的患者,【Taletrectinib】值得优先考虑。
5.PSMA阳性去势抵抗性前列腺癌:若PSMA-PET阳性,可走【Locametz筛选→Pluvicto治疗】的闭环,并在治疗过程中用PSMA-PET或【^18F-FDG PET】动态评估疗效。

(来源:摄图网)
结语:
纵览日本9月这一批批准,几乎都指向两个方向:
第一,更精准:鼻型ENK/T细胞淋巴瘤的本土证据、IDH突变脑瘤的“专病专药”、HER2/ROS1的基因分型、PSMA-PET的影像选择——从“谁该用药”开始精准,让好药用在合适的人。
第二,更前移:Pluvicto在美国已化疗前可用;Taletrectinib在中国实现了一线前移;Vorasidenib把“延缓复发”的理念带到术后早期管理。对患者来说,治疗前移=并发症后移=生存质量前移。
无论你身在国内还是计划境外就医,看到的应不只是“日本批了几款药”,而是全球证据如何被不同体系消化吸收。
这也提醒我们:MDT(多学科协作)与基因检测/分子影像将越来越成为治疗成败的“前置条件”,应尽量在初次治疗决策时就把这些步骤做足。
这一点在复杂肿瘤上尤其关键。
注:本文仅用于科普,不替代医生面诊。患者具体用药需结合分子分型、病理、影像及全身状况,由多学科团队评估后决策。
参考来源:
日本PMDA承认清单(2025年9月)
https://www.pmda.go.jp/files/000276011.pdf
【盛诺一家】成立于2011年,是国内领先的海外医疗咨询服务机构,至今已为近10000个患者家庭提供出国就医服务,重点涵盖癌症、心脏病、罕见疾病等重疾领域。凭借专业、贴心、高效的服务,盛诺一家赢得了99%客户好评率!
📌为什么出国就医患者选择盛诺一家?
- 全球就医:覆盖中、美、英、日1000家医院网络,不局限于单一国家医疗资源、规划最优就医路径
- 专业可靠:咨询服务团队成员70%拥有医学背景,包括医学院博士、三甲医院医生、资深医学翻译
- 一站式服务:在全球设有15个客户服务中心,保障从国内到海外全流程、高品质的服务质量
- 客户至上:推出48小时冷静期、风险告知书、医疗费用“零加成”等措施,保障客户权益
- 专属折扣:通过本公司预约出国就医的患者,可额外申请5%–40%的医疗费用减免折扣
👉如果您或者家人需要出国看病,可拨打免费咨询热线 400-855-7089,或通过 盛诺一家官网 预约咨询!








