每个月,日本医药与器械管理局(PMDA)都会公布当月的新批准清单。
在刚刚公布的“2025年11月新医药品承认一览”中,与肿瘤直接相关的有4条:
BRAF抑制剂Encorafenib:用于BRAF变异结直肠癌的新“一线联合方案”
TRK/ROS1抑制剂Repotrectinib:用于NTRK融合阳性实体瘤,只看基因突变、不限癌种
BCL-2抑制剂Venetoclax:扩展至慢性淋巴细胞白血病/小淋巴细胞性淋巴瘤的一线治疗
Daratumumab皮下注制剂:高风险“阴燃型多发性骨髓瘤”首个获批干预治疗
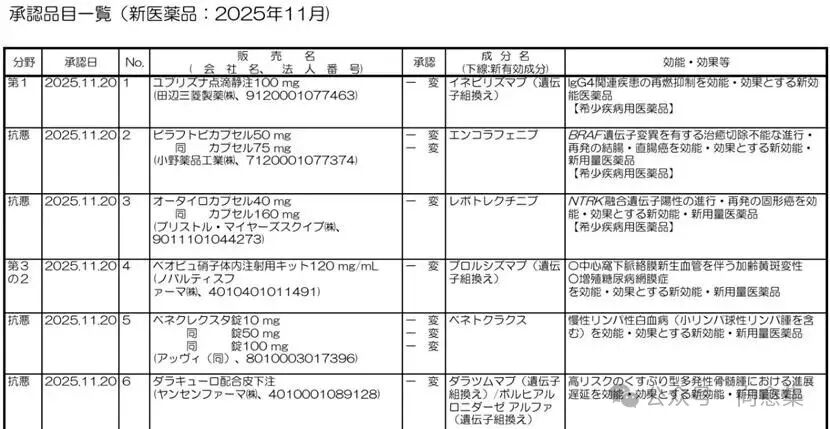
(来源:PMDA官网)
下面,我们用几分钟,把这4条新动向的关键信息装进你的脑袋。
BRAF抑制剂Encorafenib:用于BRAF变异结直肠癌的新“一线联合方案”

(来源:Array BioPharma)
获批详情:
适用人群:携带BRAF基因变异(临床上主要是V600E)的结肠癌/直肠癌患者
疾病阶段:无法根治性切除的进展期或复发期
变化性质:在日本获批新的适应证与新用量,用于这种BRAF变异结直肠癌
根据小野药品的说明,这次获批的核心是:用一套三联组合(Encorafenib + Cetuximab + FOLFOX化疗),作为BRAF变异晚期结直肠癌的一线治疗方案。
其关键临床依据来自国际III期BREAKWATER研究,面向BRAF V600E变异转移性结直肠癌,方案对比如下:
试验组:Encorafenib + Cetuximab + FOLFOX6化疗
对照组:医生选择的标准化疗(±贝伐珠单抗)
中期分析结果显示:
客观缓解率(ORR):试验组60.9%;对照组40.0%。
中位无进展生存期期:实验组约12.8个月;对照组约7.1个月。
这意味着:
试验组患者肿瘤明显缩小或消失的比例,比对照组多出近21%;
实验组患者肿瘤得到控制,没有继续变大、也没有出现新病灶的时间,比对照组延长了80%。
可以简单理解为:先用靶向药“卡”住BRAF这条异常信号链,再用化疗“收尾”;与单纯化疗相比,更容易把肿瘤压下去,维持控制时间也更长。
需要注意的是:并非人人适合“全套毒打”;三联方案“火力全开”,对体力、器官功能要求更高,高龄、体弱患者可能要个体权衡。
TRK/ROS1抑制剂Repotrectinib:用于NTRK融合阳性实体瘤,只看基因突变、不限癌种
(来源:Lucius Pharmaceutical)
什么叫“不限癌种”?
只要肿瘤细胞里有NTRK基因融合这个“异常插头”,不管肿瘤长在肺、甲状腺、唾液腺、肠道还是其他器官,一旦进入进展期或复发期,就可以考虑用Repotrectinib这类药。
临床上,其专业说法叫“肿瘤不可知(tumor-agnostic)”精准治疗:不再问“你是哪一类癌”,先问“你有没有这个基因融合”。
在日本,Repotrectinib此前已获批用于ROS1融合阳性晚期非小细胞肺癌;本次PMDA是在此基础上,增加NTRK融合阳性实体瘤,并新增160mg剂型,方便医生按推荐剂量给药。
NTRK融合非常罕见。常见实体瘤中发生率往往<1%;但一旦命中,靶向药往往效果“惊艳”,有时能达到多年缓解。
对一些儿童肿瘤、罕见腺样癌、唾液腺肿瘤等,NTRK检测尤其重要。患者就诊前建议确认:
病理是否已经做过大panel(覆盖几百甚至上千个基因检测)的NGS检测;
报告中是否明确写明“NTRK1/2/3 融合:阳性/阴性/未检出”。
BCL-2抑制剂Venetoclax:扩展至慢性淋巴细胞白血病/小淋巴细胞性淋巴瘤的一线治疗
(来源:FDA.report)
一句话解释:这是将Venclexta的适应证,从只用于“复发/难治的”慢性淋巴细胞白血病/小淋巴细胞性淋巴瘤,扩展至“一线治疗”(一确诊就可以用)。
背后的典型方案包括:
Venetoclax + Obinutuzumab(抗CD20抗体):据海外III期CLL14研究,在老年和合并症较多的慢性淋巴细胞白血病(CLL)人群中,固定12个月疗程后,可获得长期无进展生存(PFS)优势。
Venetoclax + Ibrutinib(BTK抑制剂):相关证据来自日本II期M20-353研究等,本次获批也将这一路径纳入一线选项。
它与传统治疗最大的不同在于:很多方案是“有限疗程(time-limited)”,而不是“一直吃到进展为止”。
这对患者意味着:
不一定要“长期吃药到失败”,有机会在1-2年内完成固定疗程,然后停药观察;
部分患者可获得深度分子缓解,停药后也能维持较长时间的疾病控制。
但与此同时:
起始剂量需要逐级递增,以降低肿瘤溶解综合征风险;
患者需要频繁验血、补液,甚至短期住院监测。
Daratumumab皮下注制剂:高风险“阴燃型多发性骨髓瘤”首个获批干预治疗
(来源:Multivu)
这是日本首个获批用于“高风险阴燃型多发性骨髓瘤(SMM)的进展延缓”的治疗药物。
该获批依据基于国际III期AQUILA研究。该研究采用Daratumumab皮下注射,单药治疗高风险阴燃型多发性骨髓瘤(SMM)。
所谓“阴燃型”,就是有“火”了,但还没有“烧起来、烧大”,处于相对早期。
如果把多发性骨髓瘤比喻成一场“火灾”,可以分为三个阶段:
MGUS:只有一点点烟,不确定会不会起火
SMM(阴燃期):火苗已经出现,但还没烧到房间(还没造成器官损害)
MM(骨髓瘤):火已经开始烧房子,造成明显破坏→必须马上灭火(治疗)
传统上,对于SMM(尤其是高风险),医生多采取“密切随访、观察,等到真正出现器官损害再治疗”的策略,病人常常处在“知道有个定时炸弹,却暂时不能拆”的心理煎熬中。
这次日本的做法,相当于迈出了一步:对明确属于“高风险SMM”的患者,在“真正变成多发性骨髓瘤之前”,就用药去尽量拖延疾病进展。
小结:11月清单在悄悄改变什么?
这份11月日本PMDA获批清单,给肿瘤治疗传递出的信号大致有三点:

(来源:摄图网)
1.“精准”继续加码:从BRAF变异结直肠癌,到NTRK融合实体瘤,再到慢性淋巴细胞白血病的靶向组合,越来越多方案要求:先精准分型,再谈用药。
2.“时间点”前移:慢性淋巴细胞白血病(CLL)和高风险阴燃型多发性骨髓瘤(SMM)的新方案,都在尝试更早、更有限疗程地介入,希望在损伤积累之前,抢先把疾病控制在一个相对安全的水平。
3.“罕见病群体”被更多看见:BRAF变异结直肠癌、NTRK融合实体瘤、慢性淋巴细胞白血病(CLL)/小淋巴细胞性淋巴瘤(SLL)、高风险阴燃型多发性骨髓瘤(SMM),在日本都属于 低发病率的小人群。但正因为小,更需要被“精心设计”的方案照顾到。
对患者和家属来说,比起一味“追新药”,更重要的是:先搞清楚自己到底属于哪一类、哪一小类,再去精准匹配对应的那条新闻、那款新药和疗法。
参考来源:
https://www.pmda.go.jp/files/000277965.pdf
【盛诺一家】成立于2011年,是国内领先的海外医疗咨询服务机构,至今已为近10000个患者家庭提供出国就医服务,重点涵盖癌症、心脏病、罕见疾病等重疾领域。凭借专业、贴心、高效的服务,盛诺一家赢得了99%客户好评率!
📌为什么出国就医患者选择盛诺一家?
- 全球就医:覆盖中、美、英、日1000家医院网络,不局限于单一国家医疗资源、规划最优就医路径
- 专业可靠:咨询服务团队成员70%拥有医学背景,包括医学院博士、三甲医院医生、资深医学翻译
- 一站式服务:在全球设有15个客户服务中心,保障从国内到海外全流程、高品质的服务质量
- 客户至上:推出48小时冷静期、风险告知书、医疗费用“零加成”等措施,保障客户权益
- 专属折扣:通过本公司预约出国就医的患者,可额外申请5%–40%的医疗费用减免折扣
👉如果您或者家人需要出国看病,可拨打免费咨询热线 400-855-7089,或通过 盛诺一家官网 预约咨询!








