对于晚期或转移性胆管癌患者来说,治疗选择有限、预后不佳的困境一直存在。前沿药英菲格拉替尼(Truseltiq)的出现,为患者提供了新的治疗选择。这款新型靶向药,不仅在疗效方面取得了显著突破,更为接受传统疗法治疗失败的患者提供了新的希望。那么,Truseltiq究竟是一款怎样的药?它适合哪些患者?国内患者又该如何用上?本文将从多角度进行详细解读。
来源:乐城先行区管理局发布公众号
胆管癌是一种发生在肝内外胆管或胆囊的恶性肿瘤,是一种恶性程度较高的恶性疾病。由于早期症状不明显,大多数患者确诊时已进入晚期。胆管癌患者的预后整体较差。根据博鳌超级医院数据,手术治疗后3年复发率高达85%,患者的5年生存率仅约5%[4],而无法手术切除的患者境况更困难,对放疗和化疗都不敏感。
中国每年约有72000名患者确诊为胆管癌[3]。40%的胆管癌患者存在潜在的可靶向性的基因突变[4],主要突变基因有KRAS、BRAF、FGFR2、IDH1/2等,其中FGFR2是胆管癌患者蕞常见的突变基因之一。大约14%-17%的患者存在FGFR2基因异常,这类患者的五年生存率仅为9%[3]。鉴于该疾病的严重性、缺乏高效疗法以及中国的高患病率,迫切需要为该患者群体提供更有效的新疗法。【适应症】用于治疗携带FGFR2基因融合或其他重排的、既往治疗失败的、不可切除的局部晚期或转移性胆管癌成人患者。
Truseltiq是一种靶向FGFR(成纤维细胞生长因子受体)的口服、小分子抑制剂,由美国BridgeBio Pharma公司开发。Truseltiq专门设计用于抑制FGFR2蛋白信号通路的异常活性。这种异常常见于某些类型的癌症,例如胆管癌。Truseltiq的药物作用机制是:通过靶向FGFR2的信号通路,抑制癌细胞的生长和分裂,从而抑制肿瘤的扩散和生长。这种精准的作用机制,使其在对传统疗法无效的患者中展现了显著的疗效。2021年5月28日,美国食品药品监督管理局(FDA)授予Truseltiq加速批准,用于治疗既往接受过治疗的、不可切除的局部晚期或转移性胆管癌。患者需通过FDA批准的检测方法确认存在FGFR2基因融合或其他重排。[1]2024年5月16日,美国食品药品监督管理局(FDA)正式撤销了对Truseltiq的批准。撤销并非因该药疗效不佳,主要原因为:- 原本需要在上市后进行的试验,目的是验证药物的疗效,因为招募患者太困难,导致试验无法完成。
- 药物的销售利润不够高,继续生产和推广不划算,因此研发公司自愿申请了撤回请求。
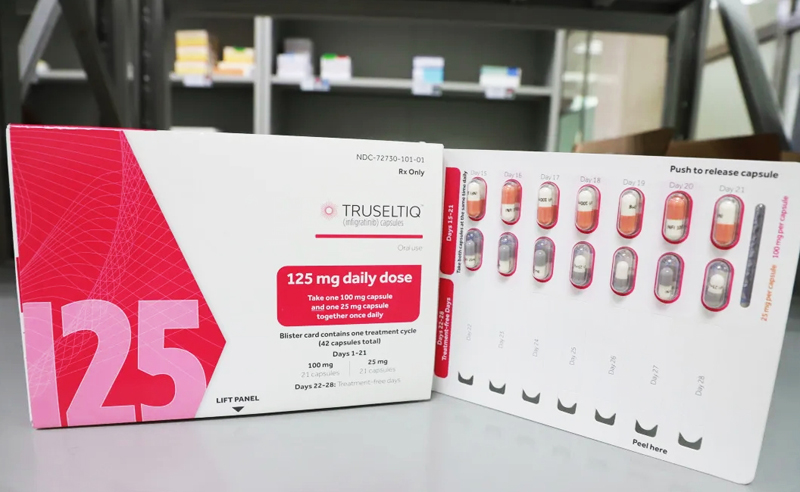
Truseltiq的有效性基于一项代号为CBGJ398X2204(NCT02150967)的2期临床试验。该试验是一项多中心、开放标签、单臂试验,招募了108名符合条件的患者。治疗方案为:患者每日口服125毫克Truseltiq,连续21天后停药7天,28天为一个周期,直至疾病进展或出现不可耐受的毒性。该研究的主要疗效指标是客观缓解率(ORR)和缓解持续时间(DOR)。
- 客观缓解率(ORR)为23%,即有23%的患者肿瘤显著缩小或完全消失。
- 在23名获得缓解的患者中,8名患者的缓解持续时间超过6个月。
Truseltiq治疗常见的不良反应(发生率≥20%)包括:
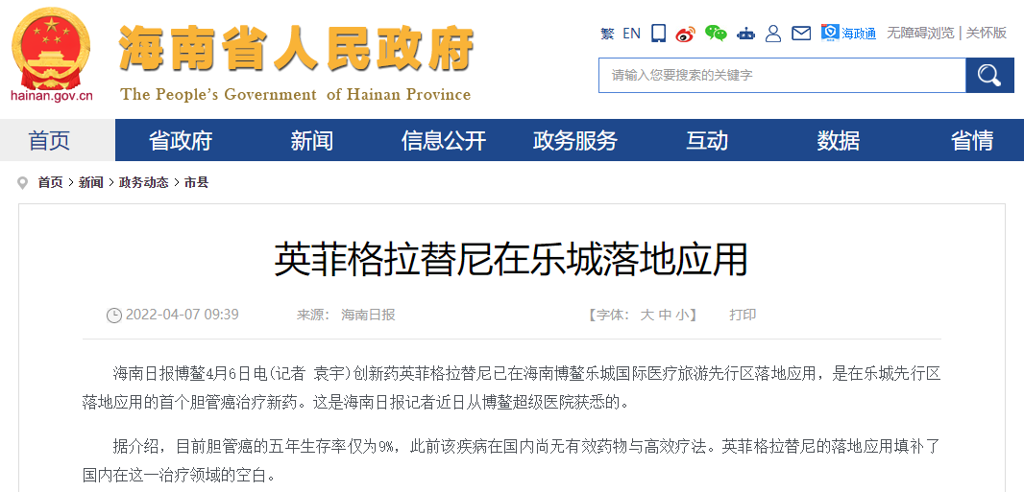
目前Truseltiq虽还未在中国获批上市,但好消息是:2022年4月,Truseltiq已在海南博鳌乐城国际医疗旅游先行区落地应用,该药也是在乐城先行区落地应用的头一款胆管癌治疗新药。[2]此前胆管癌在国内尚无有效药物与高效疗法。因此,Truseltiq的落地应用,填补了国内在这一治疗领域的空白。
2021年12月15日,头一名胆管癌患者在乐城先行区内的博鳌超级医院顺利服用英菲格拉替尼(Truseltiq),并获准“带药离园”。患者张女士(化名)四年前被诊断为肝内胆管癌,基因检测为FGFR2融合。曾接受过左半肝加胆囊切除术,进行过多次化疗、靶向治疗和免疫治疗,效果均不理想。在陷入治疗困境之际,张女士了解到在博鳌乐城可以申请使用Truseltiq,似乎看到了新的希望,于是前往申请用药。通过多学科专家的远程综合会诊,在经过专家团队的严格评估后,张女士符合用药条件,于2021年12月15日开始接受Truseltiq治疗。头一次服药后,患者的病情平稳,在确保治疗安全的情况下,为方便患者后续治疗,医院为张女士申请了“带药离园”,回家继续服用Truseltiq。用药疗效:用药3个月后,张女士的肿瘤相关指标明显改善,肿瘤缩小了近60%。[3]
2022年4月,患者杨先生在体检时发现肝肿块,经过检查确诊为胆管癌,基因检测为FGFR2-BICC1融合。确诊后杨先生即开始接受索凡替尼治疗。然而,在之后的复查中,肿瘤有所增大。面对治疗困境,杨先生的家人获知在博鳌乐城可使用国内尚未上市的Truseltiq,重燃治疗希望。经过专家团队的评估,2022年5月11日,杨先生顺利用上了Truseltiq。用药疗效:用药两个周期后,杨先生7月份的复查CT结果显示,肿瘤较之前明显缩小,评价为部分缓解(PR),指肿瘤体积缩小至少30%。用药期间,患者的耐受性总体良好,血常规、肝肾功能未见明显异常,因此,专家表示可继续使用Truseltiq进行治疗。[4]“胆管癌患者往往面临着恶性程度高、治疗难度大和生存率低的处境,针对胆管癌二线及以上患者,中国目前尚无有效的靶向治疗药物。而Truseltiq是经过临床验证的精准靶向治疗药物,有效地填补了这一治疗领域的空白。”海南博鳌超级医院消化中心主任李江峰介绍。[3]位于海南博鳌乐城国际医疗旅游先行区的海南盛诺一家诊所,可以帮助国内患者用上英菲格拉替尼(Truseltiq)。海南盛诺一家诊所成立于2020年,是正式获得海外新药急需进口申请资格的规范医疗机构。自成立以来,诊所已帮助大量国内患者“快人一步”用上了多款海外已上市、但国内尚未获批的新药、特效药。- 患者能否使用英菲格拉替尼(Truseltiq),需要先经由专门的评估,可通过提供患者的病历资料等进行线上评估;
- 使用该药,务必患者本人到海南才能使用,有着严格的用药流程,不可邮寄或家属代领;
- 该药的具体用法与用量等,需由专业医生根据患者病情进行评定。
咨询如何前往海南用上英菲格拉替尼(Truseltiq),请在线咨询。参考资料:
[1]https://www.fda.gov/drugs/resources-information-approved-drugs/withdrawn-fda-grants-accelerated-approval-infigratinib-metastatic-cholangiocarcinoma
[2]https://www.hainan.gov.cn/hainan/sxian/202204/d429268d97cb45c4afd2e3abed943511.shtml
[3]https://mp.weixin.qq.com/s?__biz=MzAwMzcxMTYwNQ==&mid=2247725810&idx=1&sn=3396f958236dcff7b3b810e00369680a&chksm=9b3bc5e8ac4c4cfe168dfa0d76e278d7dfc1c4029adfcf83d92ebc587c4156cb80aac0e0a8db&scene=27
[4]https://mp.weixin.qq.com/s?__biz=MzAwMzcxMTYwNQ==&mid=2247809809&idx=2&sn=238e489655c9af46d8b9053128aafd72&chksm=9b388c0bac4f051d117c3fb490deca58f6c644442dc7b509357801045bcc05700093d40681ae&scene=27
【盛诺一家】成立于2011年,是国内领先的海外医疗咨询服务机构,至今已为近10000个患者家庭提供出国就医服务,重点涵盖癌症、心脏病、罕见疾病等重疾领域。凭借专业、贴心、高效的服务,盛诺一家赢得了99%客户好评率!
📌为什么出国就医患者选择盛诺一家?
- 全球就医:覆盖中、美、英、日1000家医院网络,不局限于单一国家医疗资源、规划最优就医路径
- 专业可靠:咨询服务团队成员70%拥有医学背景,包括医学院博士、三甲医院医生、资深医学翻译
- 一站式服务:在全球设有15个客户服务中心,保障从国内到海外全流程、高品质的服务质量
- 客户至上:推出48小时冷静期、风险告知书、医疗费用“零加成”等措施,保障客户权益
- 专属折扣:通过本公司预约出国就医的患者,可额外申请5%–40%的医疗费用减免折扣
👉如果您或者家人需要出国看病,可拨打免费咨询热线 400-855-7089,或通过 盛诺一家官网 预约咨询!
本文为海外就医科普文章,内容仅供阅读参考,不作为任何疾病治疗的指导意见。文章由盛诺一家编译,版权归盛诺一家公司所有,转载或引用本网内容须注明“转自盛诺一家官网(www.stluciabj.cn)”字样。