导言:
美国FDA批准了头款β地中海贫血基因疗法,通过基因工程改造患者的突变基因,生成功能正常的基因,使得89%的患者至少一年不再需要输血。据悉,这款疗法售价210万美元,已远远超过了CAR-T疗法。那么到底值不值呢?具体请看下文。
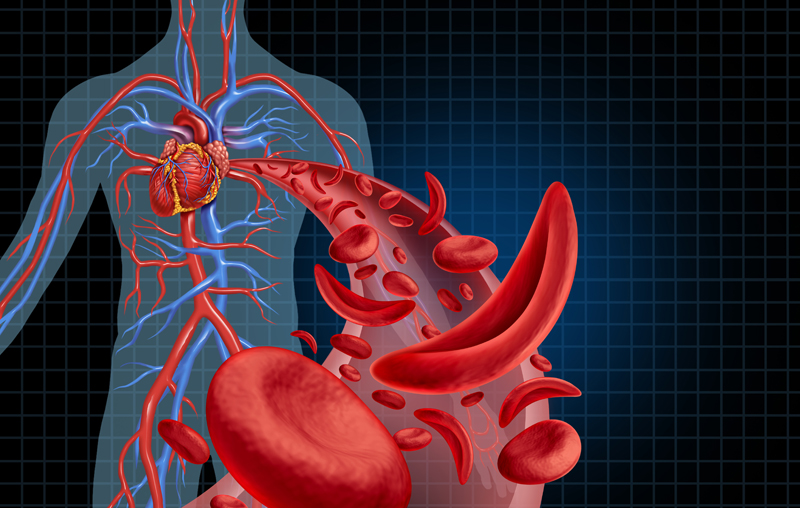
今日,美国FDA批准了Zynteglo(betibeglogene autotemcel,简称Beti-cel),治疗需要定期输血的β地中海贫血成人和儿童患者。值得一提的是,这是治疗这类患者的头一款基因疗法。
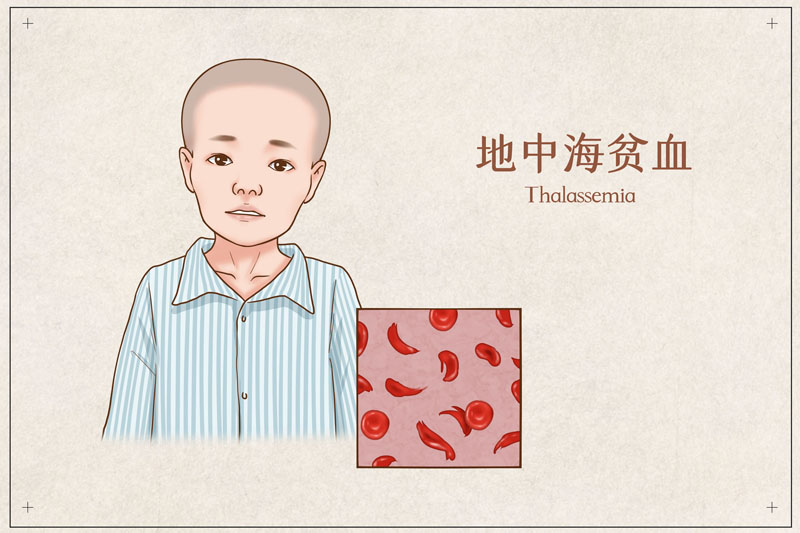
β地中海贫血是一种遗传性的血液疾病,由于存在β-珠蛋白基因突变,会造成血液里的正常血红蛋白和红细胞减少,从而导致体内氧气输送不足。红细胞水平降低会造成一系列健康问题,包括晕眩、无力、疲劳、骨髓异常等更多严重并发症。
而需要定期输血的β地中海贫血则是这类疾病中更为严重的类型,通常需要终身输血。而定期输血本身也会造成多种问题,因为体内铁过度沉积也会引起心脏、肝脏和其他器官的问题。患者平均死亡年龄为37岁。
Beti-cel是一次输注的基因疗法,每一剂都是个性化制备,使用的是患者自身的骨髓干细胞,经过基因工程改造,产生功能正常的β-珠蛋白。
Beti-cel的安全性和有效性是在两项多中心临床研究中确定的,41名4~34岁的患者接受了治疗,有效性主要看这一指标:患者维持预定的血红蛋白水平而不需要任何输血的时间至少达1年。
结果显示,在41名接受Beti-cel治疗的患者中,有89%的患者都达到了这一目标,至少一年不再需要输血。
Beti-cel治疗常见的不良反应包括血小板和其他血细胞水平降低、黏膜炎、发热性中性粒细胞减少、呕吐、发热、脱发、腹痛等。需要提醒的是,这一治疗也有造成血液肿瘤的潜在风险,不过在研究中目前均未发现。
Beti-cel在美国的预计价格为210万美元,折合人民币约1426万元。
但是一家专注于医疗成本效益分析的有影响力的非营利机构表示:“考虑到之前标准治疗需要定期输血的费用,因此新疗法的210万美元还是在可接受范围内的,并且药厂也提出如果患者在5年内需要输血,那么费用返还80%。”
该疗法预计2022年10月在美国可用。
参考资料:
[1]美国FDA官网2022年8月17日发布的《FDA Approves First Cell-Based Gene Therapy to Treat Adult and Pediatric Patients with Beta-thalassemia Who Require Regular Blood Transfusions》一文,原文链接:
https://www.fda.gov/news-events/press-announcements/fda-approves-first-cell-based-gene-therapy-treat-adult-and-pediatric-patients-beta-thalassemia-who
[2]Medscape官网2022年8月17日发布的《FDA Approves First Gene Therapy, Betibeglogene Autotemcel (Zynteglo), for Beta-Thalassemia》一文,原文链接:
https://www.medscape.com/viewarticle/979358?src=
【盛诺一家】成立于2011年,是国内领先的海外医疗咨询服务机构,至今已为近10000个患者家庭提供出国就医服务,重点涵盖癌症、心脏病、罕见疾病等重疾领域。凭借专业、贴心、高效的服务,盛诺一家赢得了99%客户好评率!
📌为什么出国就医患者选择盛诺一家?
- 全球就医:覆盖中、美、英、日1000家医院网络,不局限于单一国家医疗资源、规划最优就医路径
- 专业可靠:咨询服务团队成员70%拥有医学背景,包括医学院博士、三甲医院医生、资深医学翻译
- 一站式服务:在全球设有15个客户服务中心,保障从国内到海外全流程、高品质的服务质量
- 客户至上:推出48小时冷静期、风险告知书、医疗费用“零加成”等措施,保障客户权益
- 专属折扣:通过本公司预约出国就医的患者,可额外申请5%–40%的医疗费用减免折扣
👉如果您或者家人需要出国看病,可拨打免费咨询热线 400-855-7089,或通过 盛诺一家官网 预约咨询!








