美国FDA批准三阴性乳腺癌首款一线ADC药物Datroway!疗效优于化疗、生存期显著延长!
2026-05-26
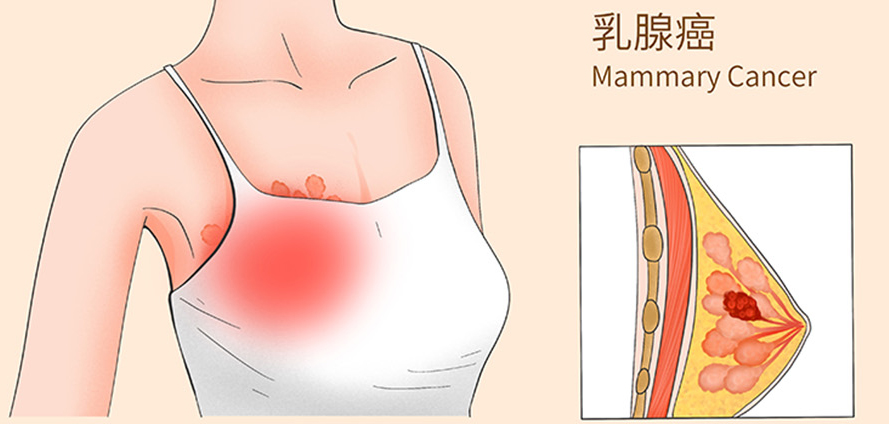
2026年5月22日,美国食品药品监督管理局(FDA)批准datopotamab deruxtecan-dlnk(商品名Datroway)用于治疗不可切除或转移性三阴性乳腺癌(TNBC)成人患者,这些患者不适合接受PD-1或PD-L1抑制剂治疗。Datroway成为首个用于这类患者一线治疗的TROP2靶向抗体偶联药物(ADC)。
曾被认为“无药可治”的癌症靶点,终于迎来突破!美国癌症研究所教授解读KRAS靶向治疗最新进展
2026-05-25
KRAS长期以来一直被认为是“无法成药”的靶点,但如今,新一代疗法正在逐渐打开局面。一些患者已经能够看到肿瘤缩小、生存期延长,而研究人员也正在努力解决耐药问题。近日,美国Karmanos癌症研究所和韦恩州立大学教授Asfar S. Azmi,在接受肿瘤资讯网站CURE®采访时,解读了KRAS是如何从曾经的“无法下手”,一步步变成如今能够被新药瞄准的治疗目标。
美国临床肿瘤学会:改写生存曲线!EV-302研究3.5年数据发布,晚期尿路上皮癌一线治疗新标准获确证
2026-05-25
一项名为EV-302(又作KEYNOTE-A39)的全球III期临床试验,在2026年美国临床肿瘤学会(ASCO)年会上公布了其新的3.5年随访结果。数据显示,对于先前未接受过治疗的局部晚期或转移性尿路上皮癌患者,Enfortumab Vedotin (Padcev)联合帕博利珠单抗(Keytruda)的治疗方案,展现了持久且卓越的生存获益,进一步巩固了其作为一线治疗新标准的地位。
美国新药前沿:子宫内膜癌迎来首个“总生存+无进展”双达标的ADC药物sac-TMT
2026-05-22
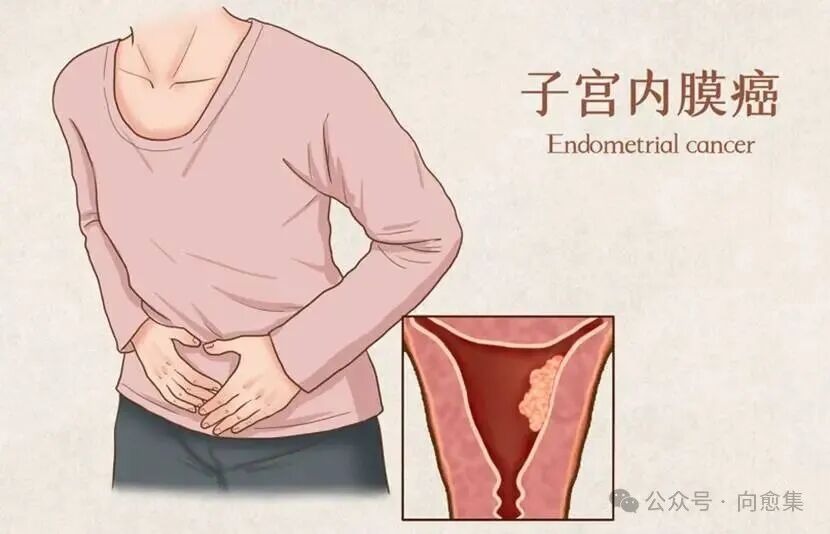
5月18日,子宫内膜癌治疗领域传来一个令人振奋的消息。默沙东宣布:一项全球III期临床研究TroFuse-005达到双主要终点,ADC药物sacituzumab tirumotecan(简称sac-TMT,中文名芦康沙妥珠单抗)在部分晚期或复发性子宫内膜癌患者中,相比化疗显著改善了两个非常关键的疗效指标,这是全球首个在这一类子宫内膜癌患者中,相比化疗同时显著改善总生存期和无进展生存期的III期研究;也是首个在这一治疗场景下实现这一结果的ADC药物。
3年超八成患者免于切膀胱:保膀胱新药Anktiva获美国FDA受理!
2026-05-22
美国食品药品监督管理局(FDA)已正式受理一款名为Nogapendekin alfa inbakicept(英文商品名:Anktiva)的膀胱癌药物的补充生物制品许可申请(sBLA)。该申请旨在扩大其使用范围,联合卡介苗(BCG),用于治疗一类特殊的非肌层浸润性膀胱癌(NMIBC)成人患者——经BCG治疗后无应答,且仅有乳头状瘤而无原位癌(CIS)的患者。FDA已将该申请的目标审评日期定为2027年1月6日。 如果获得批准,这款疗法将成为首个专门针对此类患者的、旨在保留膀胱的获批方案。
美国新药CLN-049获孤儿药资格,用于治疗复发/难治性急性髓系白血病(AML)
2026-05-21
近日,美国Cullinan Therapeutics公司宣布,美国食品药品监督管理局(FDA)已授予其开发的新药CLN-049孤儿药资格,用于治疗复发/难治性急性髓系白血病(AML)。美国FDA的孤儿药资格,是授予那些用于预防、诊断或治疗罕见疾病或罕见状况的药物和生物制品。这类疾病或状况在美国影响的人群少于20万人。孤儿药资格可使申办方获得某些研发激励。
小细胞肺癌上新药了!SNB-101给复发患者带来新希望,使83.3%患者病情得到控制
2026-05-21
根据韩国SN Biosciences公司发布的新闻稿,在一项1b/2期试验(临床试验注册号:NCT07391813)中,研究人员已经开始为首例入组患者给药。该试验正在评估新药SNB-101用于广泛期小细胞肺癌(ES-SCLC)患者的疗效。广泛期小细胞肺癌(ES-SCLC)是指癌症已扩散到肺以外的其他器官,通常进展迅速,治疗难度大。
57.1%患者肿瘤完全消失,疾病控制率高达100.0%!新药JNJ-1900治疗肺癌疗效惊艳
2026-05-21
近日,法国Nanobiotix公司在2026年欧洲放射治疗与肿瘤学会年会(ESTRO 2026)上,公布了CONVERGE研究第1部分的数据。CONVERGE研究是一项2期临床试验,正在评估新药JNJ-1900(又名NBTXR3)用于III期不可手术非小细胞肺癌(NSCLC)患者的疗效。
一项84万人的研究显示,GLP-1减重药或可帮助有肥胖或糖尿病问题的乳腺癌患者显著降复发!
2026-05-20
对很多乳腺癌患者来说,治疗结束不意味着心里的石头完全落地。经过手术、放疗、化疗、内分泌治疗等一系列治疗之后,乳腺癌患者关心的问题,莫过于降低复发风险。就在近期,发表在《JAMA Network Open》上的一项研究显示,对于同时患有肥胖或2型糖尿病的乳腺癌患者,使用GLP-1减重药(比如知名的司美格鲁肽) 后,可显著降低癌症复发风险!
针对HER2突变肺癌患者,超7成肿瘤大幅缩小!靶向药sevabertinib获美国FDA加速批准
2026-05-20
近日,美国食品药品监督管理局(FDA)授予了肺癌靶向药sevabertinib优先审评资格,用于一线治疗携带HER2基因突变的局部晚期或晚期非小细胞肺癌。Sevabertinib此前已在2025年11月获得FDA加速批准,用于治疗既往接受过治疗的晚期HER2突变非小细胞肺癌患者。也就是说,它此前的适应症主要面向“已经用过其他治疗”的患者,而这次优先审评关注的是能否将该药“前移”到一线治疗。