根据一项2a期临床试验的最终分析结果数据:美国病毒疗法CAN-2049与前药(伐昔洛韦或阿昔洛韦)及免疫检查点抑制剂(可合并或不合并化疗)联合使用,在III/IV期非小细胞肺癌(NSCLC)且对免疫治疗反应不佳的患者中,带来显著的生存期获益。
关键数据
46名可评估患者的平均总生存期为24.5个月。
在试验开始时病情出现进展的患者中,平均总生存期为21.5个月。而既往数据仅为9.8-11.8个月,几乎从未超过12个月。有37%的患者在接受CAN-2409治疗两年后仍然存活。
CAN-2049是由美国Candel Therapeutics公司开发的一款腺病毒疗法。
前药是一种本身没有活性或活性较弱的化合物,在体内经代谢转化后变为具有治疗作用的活性药物。
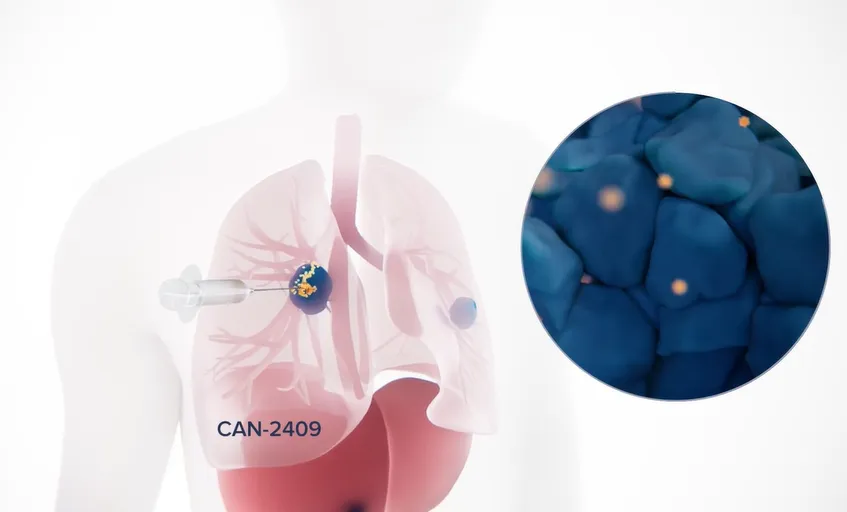
试验详情
这项单臂2期临床试验(编号NCT04495153)招募了年龄≥18岁、III/IV期NSCLC患者,所有患者均接受过免疫检查点抑制剂的一线治疗,可合并化疗。第1组要求患者在治疗18周后仍有稳定但持续存在的病灶,第2组要求影像学证实有病情进展。
其他主要入组标准包括:具有可评估的病灶,ECOG体能评分0-1(表示患者总体身体状况较好,适合参与治疗或临床试验),血液和器官功能良好,且患者在12周治疗期内需持续接受免疫检查点抑制剂治疗(入组前6个月不得更换免疫药物,且不得中断超过4周)。
在1A组和2A组中,患者接受2次CAN-2049注射,随后连续14天服用前药,并继续免疫治疗(可合并化疗);而1B组和2B组患者接受3次CAN-2049注射,但1B组中的第3次注射可根据情况给予或不给予。
该研究的主要终点为客观缓解率(肿瘤显著缩小和完全消失的患者比例)和安全性。次要终点包括总生存期、无进展生存期(从治疗开始到疾病出现进展或患者死亡的时间)和根据另一标准评估的客观缓解率。
研究结果
这项研究纳入了46名可评估患者,分为第1组和第2组。
在第1组和第2组共46名可评估患者中,平均总生存期为24.5个月。
在第2组(共41名患者)中,那些在试验开始时病情出现进展的患者,平均总生存期为21.5个月。对照以往研究显示,对于这类病情进展且接受标准治疗(如多西他赛化疗)的患者,其平均生存期通常仅为9.8-11.8个月,几乎从未超过12个月。
这次最终分析涵盖了更长的随访数据(比前一次数据分析多出一年),在可评估患者中,平均随访时间为32.4个月。
根据截至2025年3月3日的数据分析,在试验开始时病情出现进展的第2组患者中,有37%的患者在接受CAN-2409治疗两年后仍然存活。这表明该疗法可能具备“长尾效应”——即在原本预后很差的患者群体中,有相当比例的患者能获得长期生存。
补充数据显示,在有多个病灶的可评估患者中(共35名),69%的患者不仅注射部位的肿瘤缩小了,连身体其他没注射的肿瘤也跟着缩小了。表明该疗法具有激活全身免疫的潜力。
研究还发现,非鳞癌患者在免疫和临床反应方面明显优于鳞癌患者。在存活超过24个月的15名患者中,14人为非鳞癌,且在30个月时仍然存活的9人全部属于非鳞癌亚型。非鳞癌亚型患者(共33名)在使用免疫治疗后出现病情进展的情况下,接受CAN-2049治疗后,平均总生存期达到25.4个月,这一数据显著高于其他亚型。
专家评述
美国宾夕法尼亚大学佩雷尔曼医学院肺癌教授、该研究的首席研究员Charu Aggarwal博士在新闻稿中表示:“对于不可切除的NSCLC患者来说,一旦在PD-1治疗失败后,目前的治疗选择非常有限。本研究显示的生存获益令人振奋,明显优于现行标准治疗(如多西他赛)及其他正在研究中的疗法。”
Candel Therapeutics公司总裁兼首席执行官Paul Peter Tak博士表示:“此次更新的生存数据证实并加强了我们此前的研究发现,显示出CAN-2409可延长那些对免疫检查点抑制剂无效或耐药的晚期NSCLC患者的生存时间。它独特的作用机制和目前显示出的安全性,使其可能代表实体瘤治疗的一种全新方式,为改善治疗结果带来真正希望。这一具有说服力的成果,可能为攻克这种侵袭性疾病带来突破性的进展。”
未来计划
Candel Therapeutics公司宣布,这些研究数据将支持其在非鳞癌NSCLC患者中进一步开展注册性临床试验的计划。Candel Therapeutics公司将继续推进CAN-2409在NSCLC中的开发项目。
关于CAN-2049
CAN-2049是由美国Candel Therapeutics公司开发的一款在研的、即用型、复制缺陷型(指经过基因改造的腺病毒,不能在人体细胞中自行复制扩散,因此更安全)腺病毒疗法。
CAN-2049经过基因工程改造,可将单纯疱疹病毒胸苷激酶(HSV-tk)基因递送至患者的特定肿瘤部位,并诱导对肿瘤产生个体化的全身免疫应答。
HSV-tk是一种特殊的酶,它的作用是把病人吃进去的药(伐昔洛韦)在肿瘤局部“激活”,变成一种能杀死癌细胞的毒药(核苷类似物),从而杀死附近的癌细胞。
该治疗方案旨在诱导一种由CD8+ T细胞介导的个体化、特异性免疫反应,不仅作用于注射部位的肿瘤,也可作用于未注射的远端转移灶,从而发挥广泛的抗肿瘤作用。
这个原理就像“在肿瘤原地打了一针疫苗”,教身体怎么识别并攻击癌细胞。它的厉害之处在于,可以对付多种不同类型的癌细胞,不挑种类,杀伤力强。
得益于其高度适应性,CAN-2409具有治疗多种实体瘤的潜力。此前在多个临床前和临床研究中,已观察到CAN-2409作为单药使用,以及与放疗、手术、化疗、免疫检查点抑制剂等标准治疗联合使用时,具有鼓舞人心的疗效。目前已有超过1000名患者接受了CAN-2409治疗,总体表现出良好的耐受性,为其未来与其他治疗策略联合提供了支持。
CAN-2409的临床开发情况
Candel Therapeutics公司正在推进CAN-2409的临床开发计划,目前已完成多个2a期临床试验,包括非小细胞肺癌(NSCLC)和胰腺导管腺癌(PDAC)两个适应症。
此外还开展了一项关键性的、随机、安慰剂对照的3期临床试验,针对的是局部、未转移的前列腺癌。2024年12月,Candel Therapeutics公司宣布,CAN-2409在这项3期前列腺癌临床试验中达到主要终点:在中高风险局限性前列腺癌患者中,将其加入标准放疗(±雄激素剥夺治疗)后,显著改善了无病生存期(DFS,指患者接受治疗后,癌症没有复发或恶化的时间)。
在随机对照2a期胰腺导管腺癌(PDAC)研究中,结果同样令人振奋:对于“边界可切除”的胰腺癌患者,CAN-2409联合标准治疗组的预估平均总生存期为31.4个月,而对照组(仅接受标准治疗)仅为12.5个月;病情进展后患者的平均总生存期为21.2个月,而对照组仅为6.4个月。
CAN-2409已获监管认可和特殊资格
CAN-2409联合前药的治疗方案已获得美国食品药品监督管理局(FDA)授予的快速通道资格,适用于以下适应症:
胰腺导管腺癌(PDAC)
III/IV期NSCLC患者,针对PD-1和PD-L1抑制剂一线治疗无效、且无驱动基因突变或对靶向治疗耐药者。
局部原发性前列腺癌
此外,FDA还授予CAN-2409用于胰腺导管腺癌(PDAC)治疗的罕见病药物认定。
来源:
[1]https://www.onclive.com/view/can-2049-displays-potential-os-benefit-in-advanced-nsclc-after-inadequate-response-to-checkpoint-inhibitors
[2]https://ir.candeltx.com/news-releases/news-release-details/candel-therapeutics-reports-both-prolonged-median-overall
【盛诺一家】成立于2011年,是国内领先的海外医疗咨询服务机构,至今已为近10000个患者家庭提供出国就医服务,重点涵盖癌症、心脏病、罕见疾病等重疾领域。凭借专业、贴心、高效的服务,盛诺一家赢得了99%客户好评率!
📌为什么出国就医患者选择盛诺一家?
- 全球就医:覆盖中、美、英、日1000家医院网络,不局限于单一国家医疗资源、规划最优就医路径
- 专业可靠:咨询服务团队成员70%拥有医学背景,包括医学院博士、三甲医院医生、资深医学翻译
- 一站式服务:在全球设有15个客户服务中心,保障从国内到海外全流程、高品质的服务质量
- 客户至上:推出48小时冷静期、风险告知书、医疗费用“零加成”等措施,保障客户权益
- 专属折扣:通过本公司预约出国就医的患者,可额外申请5%–40%的医疗费用减免折扣
👉如果您或者家人需要出国看病,可拨打免费咨询热线 400-855-7089,或通过 盛诺一家官网 预约咨询!








