引言
免疫治疗被誉为未来很有可能治愈癌症的疗法,大家熟知的PD-1、CAR-T等,都属于免疫治疗。
近日,头个TCR疗法在美国获批,免疫治疗迎来了新的里程碑!
1月25日,美国食品与药品监督管理局批准了Kimmtrak,用于HLA-A*02:01阳性、不可切除或转移性葡萄膜黑色素瘤的成年患者。
Kimmtrak(tebentafusp-tebn)是一种新型的双特异性蛋白,由两部分融合而成,一部分是可溶性T细胞受体,与另一部分抗CD3免疫效应功能融合。Kimmtrak专门针对gp100,这是一种在黑色素细胞和黑色素瘤中表达的谱系抗原。
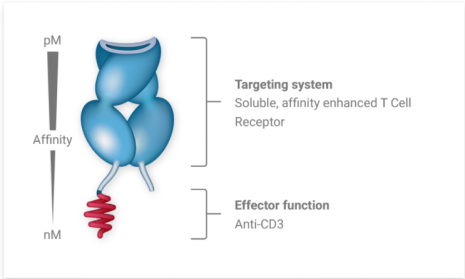
图源:Immunocore公司官网
Kimmtrak除了是头一个TCR疗法外,它还成为头一个被批准用于治疗实体瘤的BiTE免疫疗法药物,也是头一个被批准用于治疗葡萄膜黑色素瘤的药物。
UPMC Hillman癌症中心黑色素瘤中心主任、医学博士John Kirkwood说:“葡萄膜黑色素瘤是一种毁灭性的疾病,转移后患者的生存率不足一年。Kimmtrak的批准代表了转移性葡萄膜黑色素瘤治疗的重大范式转变,并头一次为患有这种侵袭性癌症的人带来了希望。”
临床试验介绍
IMCgp100-202是一项对378名转移性葡萄膜黑色素瘤患者进行了疗效评估的随机、开放标签、多中心试验。患者要求为通过中央检测鉴定的HLA-A*02:01基因型阳性。
之后,患者按照2:1的比例被随机分为两组接受用药:一组为Kimmtrak组 (N=252),另一组为研究者选择的pembrolizumab、ipilimumab或达卡巴嗪对照组(N=126)。
Kimmtrak每周通过静脉输注给药,第1天20mcg,第8天30mcg,第15天68mcg,随后每周一次,直至疾病进展或出现不可接受的毒性。
主要疗效结局指标是总生存期(OS)。另一个疗效结果是研究者评估的无进展生存期 (PFS)。
接受Kimmtrak治疗的患者的中位OS为21.7个月,对照组为16个月;接受Kimmtrak治疗的患者PFS为3.3个月,对照组为2.9个月。
Immunocore首席执行官Bahija Jallal说:“Kimmtrak 是头一个证明对患有这种疾病的患者有生存益处的疗法,我们专注于尽快使它能被患者用上。”
IMCgp100-202试验结果不仅是葡萄膜黑色素瘤的里程碑,也是一般癌症免疫疗法的里程碑,因为它是头一个在实体瘤中显示出明显优于PD1/PD-L1抑制剂的关键研究。
来源:
[1]https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-tebentafusp-tebn-unresectable-or-metastatic-uveal-melanoma
[2]https://pharmaphorum.com/news/immunocore-claims-first-ever-fda-approval-for-tcr-cancer-therapy/
[3]https://ir.immunocore.com/news-releases/news-release-details/immunocore-announces-fda-approval-kimmtrakr-tebentafusp-tebn
[4]https://www.immunocore.com/our-therapy-areas/oncology
【盛诺一家】成立于2011年,是国内领先的海外医疗咨询服务机构,至今已为近10000个患者家庭提供出国就医服务,重点涵盖癌症、心脏病、罕见疾病等重疾领域。凭借专业、贴心、高效的服务,盛诺一家赢得了99%客户好评率!
📌为什么出国就医患者选择盛诺一家?
- 全球就医:覆盖中、美、英、日1000家医院网络,不局限于单一国家医疗资源、规划最优就医路径
- 专业可靠:咨询服务团队成员70%拥有医学背景,包括医学院博士、三甲医院医生、资深医学翻译
- 一站式服务:在全球设有15个客户服务中心,保障从国内到海外全流程、高品质的服务质量
- 客户至上:推出48小时冷静期、风险告知书、医疗费用“零加成”等措施,保障客户权益
- 专属折扣:通过本公司预约出国就医的患者,可额外申请5%–40%的医疗费用减免折扣
👉如果您或者家人需要出国看病,可拨打免费咨询热线 400-855-7089,或通过 盛诺一家官网 预约咨询!








